Spis treści
- 1. Wprowadzenie
- 2. Charakterystyka i mechanizmy działania wód głębinowych pod kątem wpływu na przewód pokarmowy
- 3. Przegląd dowodów klinicznych
- 4. Interpretacja dowodów klinicznych w kontekście zaprać, wzdęć i niestrawności
- 5. Ograniczenia
- 6. Podsumowanie
- Bibliografia
1. Wprowadzenie
Problemy żołądkowo-jelitowe, tj. przewlekłe zaparcia czynnościowe, wzdęcia czy szeroko rozumiana niestrawność, stanowią częsty problem w praktyce gastroenterologicznej i dietetyce klinicznej a ich patofizjologia obejmuje złożone interakcje pomiędzy motoryką jelit, składem mikrobioty, procesami fermentacyjnymi, integralnością bariery śluzówkowej oraz zaangażowaniem w procesy trawienne osi jelito-mózg. Wobec złożonej patofizjologii zaburzeń czynnościowych przewodu pokarmowego rośnie znaczenie interwencji, które działają wielokierunkowo — nie tylko na samą perystaltykę, ale także na środowisko mikrobiotyczne, równowagę elektrolitową oraz mechanizmy adaptacyjne śluzówki. W ostatnich latach obserwuje się rosnące zainteresowanie kwestiami spożywanej wody, nie tylko pod kątem odpowiedniej ilości przyjmowanych płynów, ale także pod względem ich składu mineralnego.
Głębinowa woda morska (ang. Deep Sea Water, DSW) pozyskiwana jest z głębokości sięgających kilkuset metrów, gdzie środowisko cechuje niska temperatura, wyjątkowa czystość, stabilność termiczna i minimalne zanieczyszczenie chemiczne oraz biologiczne. DSW wyróżnia się parametrami nie obserwowanymi w typowych wodach butelkowanych: tj. nie zawiera węglowodanów, tłuszczów, białek ani innych bioaktywnych substancji ale posiada specyficzny skład chemiczny i profil jonowy, determinowany przez długotrwały obieg wody w głębokich warstwach oceanicznych. Charakterystyczny profil jonowy jest związany z wyjątkowo wysoką zawartością magnezu, potasu, wapnia i pierwiastków śladowych, takich jak lit i jod, specyficzną proporcją Mg:Ca, odmienną od tej, którą obserwuje się w wodach powierzchniowych i standardowych wodach mineralnych oraz wysoką twardością (około 300 mg CaCO₃/L), wynikającą z dominacji magnezu w składzie [1].
Przeprowadzone dotychczas badania naukowe wykazują, że skład mineralny wody – zwłaszcza pochodzącej z głębin oceanicznych (ang. deep-sea water, DSW) – wywiera działanie hipocholesterolemiczne i przeciwmiażdżycowe przez modulację metabolizmu lipidów, zmniejsza ryzyko wystąpienia nadciśnienia, otyłości, cukrzycy i zaćmy a także jest korzystny dla osób z chorobami układu krążenia, ponieważ może zmniejszyć ryzyko zawału serca poprzez rozszerzenie naczyń krwionośnych i zatrzymanie skurczów mięśnia sercowego [2]. Zgromadzone dane przedkliniczne wykazały, że spożywanie wody głębinowej sprzyja regulacji motoryki jelit, wspiera funkcjonowanie bariery nabłonkowej, wpływa na przewodnictwo elektrolitowe oraz aktywność enzymów trawiennych poprawiając funkcjonowanie całego przewodu pokarmowego, co czyni DSW naturalnym, wieloskładnikowym źródłem o potencjalnie korzystnym wpływie na czynność przewodu pokarmowego.
W niniejszym rozdziale przedstawiono analizę wyników dwóch randomizowanych badań klinicznych, przeprowadzonych w schemacie podwójnego zaślepienia, w których oceniano wpływ spożywania wód głębinowych na parametry środowiska jelitowego i złagodzenie objawów ze strony przewodu pokarmowego.
2. Charakterystyka i mechanizmy działania wód głębinowych pod kątem wpływu na przewód pokarmowy
Ekosystem jelitowy stanowi złożony układ obejmujący mikrobiotę, metabolity pochodzenia mikrobiotycznego oraz treść pokarmową, a także sieć interakcji pomiędzy mikroorganizmami (ang. microbe-microbe) oraz między gospodarzem a mikroorganizmami (ang. host-microbe). Struktura ta pełni fundamentalną rolę w utrzymaniu homeostazy ustroju ludzkiego i odgrywa zasadniczą rolę w etiopatogenezie licznych schorzeń, w tym zaburzeń neuropsychiatrycznych [3].
Na skład i funkcjonowanie ekosystemu jelitowego istotnie wpływają różnorodne czynniki środowiskowe i behawioralne, takie jak warunki życia, tryb pracy, higiena snu, przewlekły stres czy sposób odżywiania. W celu modulacji i podtrzymania równowagi mikrobiologicznej w środowisku jelitowym powszechnie stosuje się probiotyki, prebiotyki oraz żywność funkcjonalną i prozdrowotną, w tym produkty z roślin strączkowych. Mikroorganizmy jelitowe wytwarzają metabolity, takie jak izoflawony, których zawartość różni się u poszczególnych osób ze względu na różnice w środowisku jelitowym, w tym tożsamość i aktywność mikrobiologiczną, stabilność oraz zmienność stężeń związków endogennych, które modulują szlaki biotransformacji [4].
Drobnoustroje jelitowe wytwarzają liczne metabolity, w tym izoflawony. Ekwol stanowi metabolit izoflawonu sojowego – daidzeiny – i wykazuje najsilniejsze spośród wszystkich izoflawonów działanie fizjologiczne na organizm gospodarza. Jego biosynteza jest uzależniona od obecności specyficznych szczepów bakterii jelitowych, w związku z czym poziom ekwolu w organizmie pozostaje ściśle zależny od mikrośrodowiska jelitowego[5]. Jednym z aktualnych kierunków badań jest poszukiwanie sposobów modulacji ekosystemu jelitowego w celu zwiększenia endogennej produkcji ekwolu.
W kontekście poszukiwania interwencji zdolnych do modyfikowania ekosystemu jelitowego coraz większą uwagę zwraca się na właściwości wód głębinowych, których unikalny profil mineralny wykazuje wielokierunkowy wpływ na mikrobiotę i funkcję bariery jelitowej. Wyniki badań przedklinicznych wskazują, że DSW może łagodzić stan zapalny jelit, normalizować przepuszczalność nabłonka, redukować stres oksydacyjny oraz działać przeciwbakteryjnie modulując skład mikrobioty w kierunku wzrostu bakterii produkujących krótkołańcuchowe kwasy tłuszczowe.
Wyniki badania Park i wsp. (2023), przeprowadzonego na szczurach, wskazują na znaczącą poprawę uszkodzenia błony śluzowej żołądka i zwiększenie jej grubości po spożyciu wody mineralnej na bazie wody głębinowej. Wyniki te jednoznacznie potwierdziły hipotezę, że woda głębinowa dzięki specyficznemu stężeniu jonów magnezu, poprzez zwiększenie ekspresji COX-1 i COX-2 oraz wzrost syntezy prostaglandyny E2 (PGE2), posiada potencjał zapobiegania powstawaniu wrzodów oraz wspiera produkcję śluzu [6].
Z kolei wyniki badania przeprowadzonego przez Yang i wsp. (2014) wykazały, że DSW cechuje się silniejszą aktywnością w wychwytywaniu reaktywnych form tlenu (H₂O₂ i HOCl) i bezpośrednio je neutralizuje, indukuje ekspresję genów i białek o działaniu antyoksydacyjnym (Txnrd1) i antyapoptotycznym (Bcl-2) oraz prowadzi do zmniejszenia ekspresji genów proapoptotycznych w nabłonku dwunastnicy. Wyniki in vivo potwierdziły, że spożycie DSW redukowało powierzchnię owrzodzeń dwunastnicy indukowanych kwasem octowym oraz liczbę komórek apoptotycznych, z zaangażowaniem szlaku Bax/Bcl-2/kaspaza 3/PARP [7]. Co istotne, badanie Yang i wsp. (2014) to pierwsze badanie, które wykazało, że DSW może bezpośrednio wychwytywać reaktywne formy tlenu (ROS) oraz zwiększać ekspresję genów oraz białek antyoksydacyjnych i antyapoptotycznych w nabłonku dwunastnicy poprzez działanie selenu, ale nie MgCl2.
Z perspektywy fizjologii przewodu pokarmowego, a w szczególności w kontekście zaparć czynnościowych i wzdęć, kluczowe znaczenie mogą mieć następujące mechanizmy biologiczne wynikające ze specyficznego profilu jonowego DSW:
- modulacja motoryki jelit poprzez działanie osmotyczne jonów magnezu i wapnia, wpływ na przewodnictwo jonowe mięśni gładkich oraz stymulację hormonów regulujących perystaltykę, takich jak cholecystokinina i motylina;
- modulacja składu i aktywności mikrobioty jelitowej, szczególnie poprzez zwiększenie produkcji krótkołańcuchowych kwasów tłuszczowych (SCFA), takich jak kwas octowy, propionowy i masłowy, które wykazują działanie troficzne na kolonocyty, a tym samym wzmacniają lokalną homeostazę energetyczną oraz wpływają na modulację perystaltyki jelit;
- wzmocnienie bariery jelitowej i odporności lokalnej poprzez zwiększenie sekrecji immunoglobuliny A (sIgA), co może redukować translokację bakteryjną i wtórny stan zapalny błony śluzowej oraz stabilizować funkcję nabłonka jelitowego;
- zmniejszenie produkcji toksycznych metabolitów bakteryjnych (np. fenolu, indolu), które sprzyjają rozwojowi dysbiozy, nasilają fermentację gnilną i mogą powodować objawy dyspeptyczne oraz wzdęcia.
Choć większość mechanizmów pozostaje hipotezą, powyższe kierunki pozwalają zrozumieć, dlaczego spożycie wód głębinowych może wykazywać pozytywne efekty w obrębie przewodu pokarmowego. Tak ukierunkowane działania wynikające ze specyficznego profilu mineralnego głębinowej wody morskiej stanowią podstawę do oceny jej roli jako naturalnego modulatora czynności przewodu pokarmowego, co znalazło odzwierciedlenie w badaniach klinicznych analizowanych w dalszej części rozdziału.
3. Przegląd dowodów klinicznych
Podczas systematycznego przeszukiwania medycznych baz danych zidentyfikowano dwa randomizowane, podwójnie zaślepione, kontrolowane badania kliniczne, których celem była analiza wpływu spożywania rafinowanej wody głębinowej (ang. rafined deep-sea water, RDSW) (Takeuchi i wsp., 2020) oraz wody pitnej (MIU) na bazie głębinowej wody morskiej (Tekeuchi i wsp., 2022) na ekosystem jelitowy człowieka.
3.1. Metodologia
Projekt badania: Oba zidentyfikowane badania kliniczne, były badaniami randomizowanymi, kontrolowanymi, prowadzone w schemacie podwójnego zaślepienia. Celem badania Takuchi i wsp. (2020) była ocena ekosystemu jelitowego u osób spożywających rafinowaną wodę głębinową (RDSW), natomiast w badaniu Takeuchi i wsp. (2022) oceniano wpływ na zdrowie jelit wody pitnej (MIU) na bazie głębinowej wody morskiej (ang. deep-sea water, DSW). W obu badaniach grupę kontrolną stanowili pacjenci spożywający wodę mineralną. Oceny dokonano na podstawie kwestionariusza do samodzielnego wypełnienia przez uczestników oraz analizy próbek kału i moczu, które zbierano przed oraz po interwencji. Badania przeprowadzono odpowiednio w latach 2016–2018 i 2018-2020 w Muroto w Japonii.
Populacja pacjentów: Do badania Takeuchi i wsp. (2020) włączono łącznie 115 uczestników, z kolei do badania Takeuchi i wsp. (2022) – 114 zdrowych, dorosłych uczestników, którzy złożyli pisemną zgodę na udział w badaniu. Osoby z jakąkolwiek obecną chorobą w chwili włączenia do badania bądź chorujące przewlekle, przyjmujące leki na receptę lub komercyjnie dostępne preparaty nie spełniały kryteriów włączenia do badania. Z badania wykluczono również kobiety będące w ciąży oraz osoby stosujące jakiekolwiek suplementy diety.
Po uzyskaniu pisemnej świadomej zgody, 98 zdrowych dorosłych uczestników w badaniu Takeuchi i wsp. (2020) zostało losowo przydzielonych do dwóch grup terapeutycznych: grupy spożywającej rafinowaną wodę głębinową (RDSW; n=49) oraz grupy kontrolnej, spożywającej wodę mineralną (n=49). W badaniu Takuechi i wsp. (2022), spośród 107 zdrowych dorosłych, którzy spełnili kryteria włączenia, 82 uczestników, którzy prawidłowo wypełnili kwestionariusz, losowo podzielono do dwóch grup: grupy badawczej MIU, tj. grupy spożywającej wodę pitną na bazie głębinowej wody morskiej (n=41) i grupę kontrolną, spożywającą jedynie wodę mineralną (n=41).
Interwencja: W obu przytoczonych badaniach wykorzystano odpowiednio butelkowaną rafinowaną wodę głębinową (RDSW) oraz wodę pitną MIU (Dydo-miu; Dydo-Takenaka Beverage Co., Ltd., Kochi, Japan) na bazie głębinowej wody morskiej (DSW). Oba rodzaje wody nie zawierały kalorii, białka, tłuszczu, węglowodanów ani witamin. Grupę kontrolną stanowiła grupa uczestników spożywająca komercyjnie dostępną wodę mineralną. Woda RDSW i MIU charakteryzowała się wysoką twardością (typ hard, w przypadku wody MIU twardość na poziomie 88), natomiast woda mineralna – niską twardością (typ soft, z twardością na poziomie 0-20). Uczestnicy w obu badaniach spożywali 1 litr przypisanego rodzaju wody dziennie przez okres 12. tygodni.
Punkty końcowe: W celu oceny ogólnego stanu zdrowia uczestników wprowadzono ankietę do samodzielnego wypełnienia. Pytania dotyczyły ogólnego stanu zdrowia jelit i nawyków żywieniowych, dyskomfortu w jamie brzusznej, stosowanych leków oraz spożywania nietypowych pokarmów i napojów. Definicję zaparcia przyjęto zgodnie z kryteriami World Gastroenterology Organization (WGO). W pobranych próbkach kału przeanalizowano następujące biomarkery: wydzielniczą immunoglobulinę A (sIgA), pięć produktów gnilnych (fenol, p-krezol, 4-etylofenol, indol i skatol) oraz dziewięć krótkołańcuchowych kwasów tłuszczowych SCFA: kwas bursztynowy, mlekowy, mrówkowy, octowy, propionowy, izomasłowy, masłowy, 3-metylomasłowy i walerianowy. W próbkach moczu oznaczano poziom trzech izoflawonów: genisteiny, daidzeiny i ekwolu.
Analiza statystyczna: W trakcie badania przeprowadzono analizy statystyczne z wykorzystaniem testów nieparametrycznych, chyba że wskazano inaczej. Dane dotyczące biomarkerów w obu badaniach analizowano z zastosowaniem metod nieparametrycznych z zastosowaniem testu U Manna–Whitneya, w celu oceny różnic pomiędzy wartościami uzyskanymi przed i po zastosowanej interwencji. Normalność rozkładu danych oceniano za pomocą testu Kołmogorowa–Smirnowa. Wartości pomiarowe przed i po zastosowaniu interwencji oceniano dla wszystkich biomarkerów w obu grupach terapeutycznych za pomocą testu rang Wilcoxona (p<0,05). W obu badaniach, w przypadku biomarkerów kałowych z analizy statystycznej wykluczono kwas mrówkowy ze względu na niewielką liczebność próbek. Na podstawie różnic w zmianach stężeń biomarkerów kałowych podczas stosowania interwencji przeprowadzono analizę regresji logistycznej wielorakiej w celu oceny zależności pomiędzy rodzajem spożywanej wody a biomarkerami kałowymi (p<0,05). Analizę tę wykonano na odpowiednio oczyszczonych danych, z wyłączeniem wartości odstających.
3.2. Wyniki
3.2.1. Badanie Takeuchi i wsp. (2020)[8]
3.2.1.1. Kwestionariusz do samodzielnego wypełnienia
Kwestionariusz (n=98) wykazał, że zgodnie z przyjętą definicją zaparcia, przed rozpoczęciem badania dolegliwość tę zgłaszało odpowiednio 17 uczestników z grupy stosującej RDSW oraz 15 uczestników z grupy kontrolnej, spożywającej wodę mineralną. Podczas trwania badania wykazano, że u 16 z 17 osób (94%) w grupie badanej oraz u 9 z 15 osób (60%) w grupie kontrolnej nastąpiło złagodzenie zaparć. Odsetek osób ze znaczną poprawą samopoczucia wynikającą ze zmniejszenia dolegliwości był istotnie statystycznie wyższy w grupie spożywającej rafinowaną wodę głębinową w porównaniu z grupą kontrolną (p<0,05).
3.2.1.2. Analiza stężeń sIgA i produktów gnilnych w próbkach kału
Z analizy próbek kału wykluczono trzech uczestników z grupy kontrolnej z powodu niewystarczającej ilości materiału biologicznego. Ostatecznie do analizy włączono próbki pochodzące od 49 osób przyjmujących RDSW oraz 46 osób z grupy kontrolnej. W grupie uczestników przyjmujących RDSW odnotowano istotne statystycznie obniżenie stężeń sIgA oraz fenolu po zakończeniu stosowania interwencji. W grupie kontrolnej nie stwierdzono istotnych statystycznie różnic pomiędzy wartościami przed i po stosowaniu interwencji. Średnie wartości stężeń sIgA i produktów gnilnych w kale w obu grupach terapeutycznych w trakcie stosowania interwencji zestawiono w poniższej tabeli.
Tabela 1. Średnie wartości stężenia sIgA i produktów gnilnych w kale w obu grupach terapeutycznych przed i po zastosowaniu interwencji (źródło: Takeuchi i wsp., 2020).
zastosowaniem interwencji
zastosowaniu interwencji
zastosowaniem interwencji
zastosowaniu interwencji
* p<0,05; ** p<0,01; ↓ – spadek.
3.2.1.3. Analiza stężeń krótkołańcuchowych kwasów tłuszczowych (SCFA) w próbkach kału
Analiza wykazała, że po zakończeniu przyjmowania interwencji w grupie uczestników przyjmujących RDSW istotnie wzrosły stężenia pięciu kwasów: bursztynowego, mlekowego, octowego, izomasłowego oraz 3-metylomasłowego (p<0,05). Dla porównania, w grupie kontrolnej stężenia dwóch biomarkerów – kwasu octowego i propionowego – istotnie obniżyły się po zakończeniu przyjmowania wody mineralnej. Łączna zawartość dziewięciu SCFA wzrosła w grupie uczestników przyjmujących RDSW z 5,81 do 6,30 mg/g, natomiast w grupie kontrolnej zmniejszyła się z 5,92 do 5,05 mg/g. Suma SCFA po zakończeniu stosowania interwencji była istotnie wyższa w grupie uczestników przyjmujących RDSW w porównaniu z grupą kontrolną, co odpowiadało różnicy na poziomie 23% między grupami.
W oparciu o różnice w zmianach stężeń biomarkerów kałowych w przebiegu interwencji, przeprowadzono analizę regresji logistycznej wielorakiej w celu oceny zależności pomiędzy rodzajem spożywanej wody a poziomami biomarkerów kałowych. Analiza wykazała, że spożycie RDSW istotnie wpływało jedynie na dwa biomarkery – kwas octowy i kwas 3-metylomasłowy. Średnie wartości stężeń krótkołańcuchowych kwasów tłuszczowych (SCFA) w kale w obu grupach terapeutycznych w trakcie stosowania interwencji zestawiono w poniższej tabeli.
Tabela 2. Średnie wartości stężeń krótkołańcuchowych kwasów tłuszczowych (SCFA) w kale w obu grupach terapeutycznych w trakcie stosowania interwencji (źródło: Takeuchi i wsp., 2020).
zastosowaniem interwencji
zastosowaniu interwencji
zastosowaniu interwencji
* p<0,05; ** p<0,01; ↑ – wzrost; ↓ – spadek; ^ kwas mrówkowy został wykluczony z analizy. SCFA – krótkołańcuchowe kwasy tłuszczowe (ang. short-chain fatty acids, SCFA).
Dla wszystkich SCFA (z wyjątkiem kwasu mrówkowego) odsetek uczestników, u których po zakończeniu stosowania interwencji odnotowano wzrost stężenia (tzw. responders) był wyższy w grupie badanej niż w grupie kontrolnej. Istotną statystycznie różnicę pomiędzy grupami zaobserwowano jedynie w przypadku kwasu octowego.
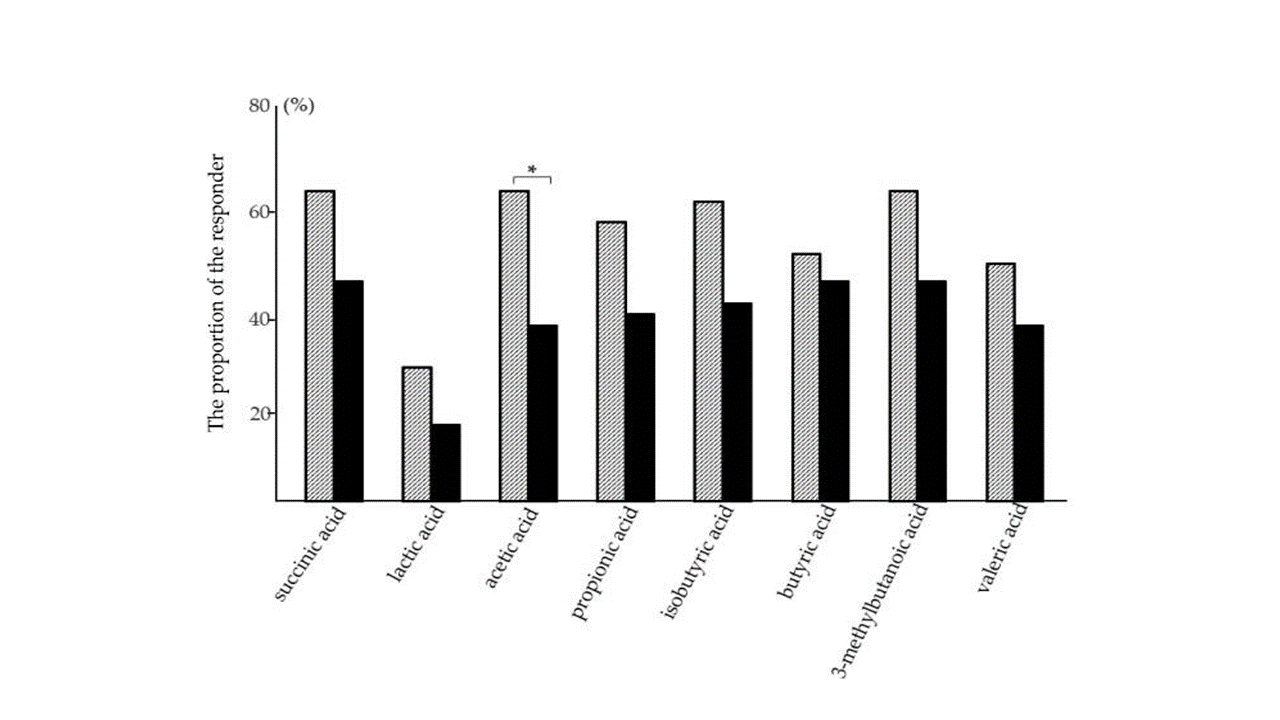
Rycina 1. Odsetek uczestników, u których po zastosowaniu interwencji odnotowano wzrost stężenia ośmiu krótkołańcuchowych kwasów tłuszczowych (SCFA) (źródło: Takeuchi i wsp., 2020). Słupek kreskowany – grupa badana, przyjmująca RDSW; słupek czarny – grupa kontrolna, przyjmująca wodę mineralną.
Uzyskane wyniki wskazują, że spożywanie rafinowanej wody głębinowej (RDSW) w sposób bardziej wyraźny stymuluje produkcję SCFA w ekosystemie jelitowym człowieka niż spożywanie wody mineralnej. Kwas mrówkowy wykryto jedynie w próbkach od 5 spośród 95 uczestników, w zakresie 0,01–0,02 mg/mL (granica detekcji: 0,01 mg/mL), co sugeruje, że w jelicie człowieka powstają jedynie śladowe ilości tego związku.
3.2.1.4. Analiza stężeń izoflawonów w moczu
Z analizy stężenia izoflawonów w moczu wykluczono próbki moczu od jednego uczestnika z każdej grupy terapeutycznej z powodu niewystarczającej objętości materiału. Ostatecznie do analizy włączono próbki od 48 uczestników spożywających RDSW oraz 48 z grupy kontrolnej, przyjmującej wodę mineralną. W moczu dwóch uczestników z grupy RDSW nie wykryto daidzeiny, natomiast genisteiny nie wykryto u jednego uczestnika w każdej z grup terapeutycznych. U jednego uczestnika z grupy RDSW nie stwierdzono obecności ani daidzeiny, ani genisteiny. Łączny współczynnik wykrywalności obu izoflawonów w próbkach moczu wyniósł 97% (93/96). Ekwol wykryto w moczu 19 uczestników z grupy RDSW oraz 17 uczestników z grupy kontrolnej, co oznacza, że ogółem 38% badanych (36/96) stanowiło producentów ekwolu.
W poniższej tabeli przedstawiano wskaźniki wykrywalności izoflawonów w moczu. W przypadkach, gdy izoflawony nie były wykrywalne, ich stężenie przyjmowano jako zero.
Tabela 3. Wskaźniki wykrywalności izoflawonów w moczu w obu grupach terapeutycznych w trakcie stosowania interwencji (źródło: Takeuchi i wsp., 2020).
* z uwzględnieniem trzech uczestników, u których daidzeina została wykryta w próbkach w co najmniej jednym punkcie czasowym badania; ** z uwzględnieniem jednego uczestnika, u którego daidzeina została wykryta w próbkach w co najmniej jednym punkcie czasowym interwencji; ^ U jednego uczestnika nie wykryto ani genisteiny, ani daidzeiny; # z uwzględnieniem trzech uczestników, u których ekwol został wykryty w próbkach w co najmniej jednym punkcie czasowym interwencji; $ z uwzględnieniem jednego uczestnika, u którego ekwol został wykryty w próbkach w co najmniej jednym punkcie czasowym interwencji.
Średnie zmiany stężeń trzech izoflawonów w trakcie stosowania interwencji porównano pomiędzy grupami. Skorygowane względem kreatyniny stężenia daidzeiny i genisteiny wzrosły w grupie uczestników przyjmujących RDSW odpowiednio o 1,44 i 1,05, natomiast w grupie kontrolnej odnotowano ich spadek o -0,14 i -0,39. Stężenia ekwolu analizowano u 16 uczestników z każdej grupy, po wykluczeniu trzech osób z grupy RDSW i jednej osoby z grupy kontrolnej z powodu braku wykrycia daidzeiny w którymkolwiek punkcie czasowym podczas przyjmowania interwencji. Średnie stężenie ekwolu wzrosło w obu grupach — o 0,42 w grupie RDSW i o 0,18 w grupie kontrolnej. Produkcja ekwolu w grupie RDSW była co najmniej dwukrotnie wyższa niż w grupie kontrolnej, jednak różnica ta nie osiągnęła istotności statystycznej. (Rycina 2).
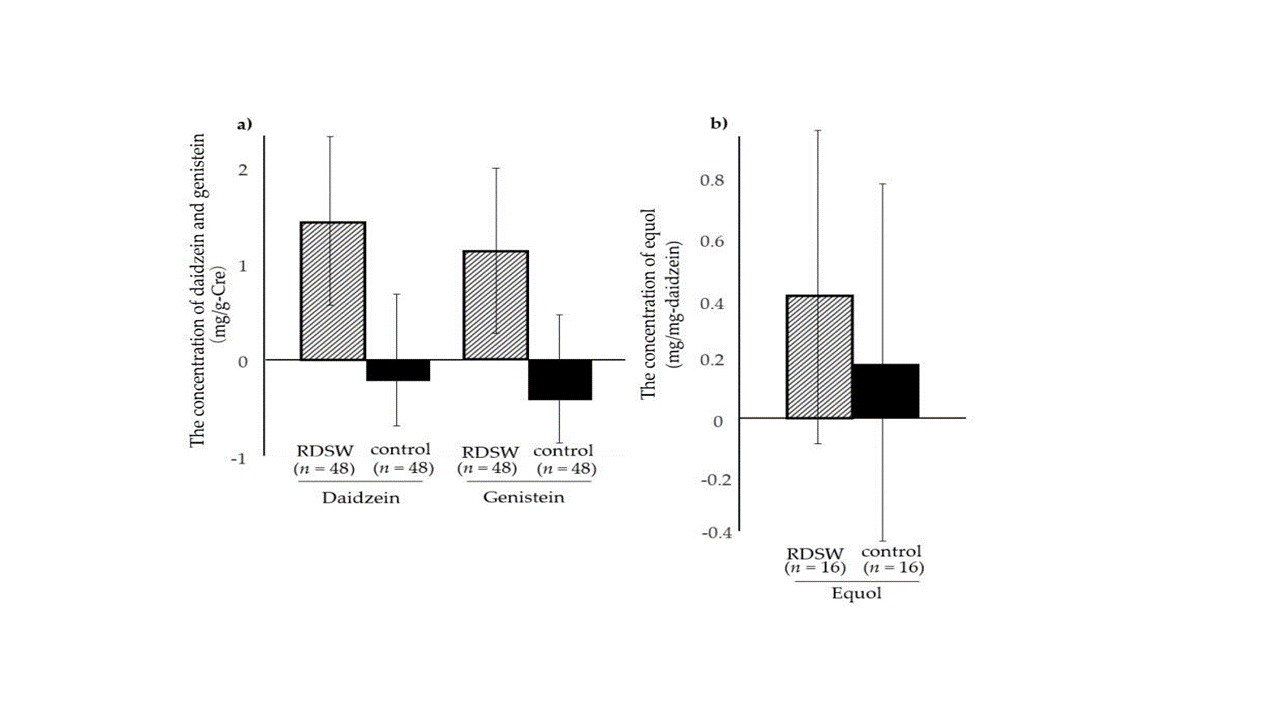
Rycina 2. Różnica stężeń izoflawonów w moczu w obu grupach terapeutycznych w trakcie stosowania interwencji: a) daidzeina i genisteina, b) ekwol (źródło: Takeuchi i wsp., 2020). Słupki przedstawiają błąd standardowy (ang. standard error, SE). Słupek kreskowany – grupa badana, przyjmująca RDSW; słupek czarny – grupa kontrolna, przyjmująca wodę mineralną.
Wyniki badania Takieuchi i wsp. (2020) wykazały, że spożywanie wody RDSW było korzystniejsze niż picie konwencjonalnej wody mineralnej. Zaparcia zostały złagodzone w znacznie większym stopniu w grupie pacjentów spożywających RDSW, czemu towarzyszyła zwiększona produkcja krótkołańcuchowych kwasów tłuszczowych (SCFA) w kale i izoflawonów w moczu, niż w grupie kontrolnej stosującej wodę mineralną.
3.2.2. Badanie Takeuchi i wsp. (2022) [9]
3.2.2.1. Kwestionariusz do samodzielnego wypełnienia
Do wypełnienia kwestionariusza przystąpiło łącznie 86 uczestników, w tym 4 osoby, które nie oddały próbek moczu i kału. Analiza kwestionariusza (n=86) wykazała, że zgodnie z przyjętą definicją zaparcia, przed rozpoczęciem badania dolegliwość tę zgłaszały odpowiednio 3 osoby z grupy badawczej i 2 z grupy kontrolnej. Podczas trwania badania wykazano, że picie wody złagodziło tą dolegliwość u wszystkich osób w grupie badanej (100%), przyjmujących wodę głębinową, i nie wykazało żadnego wpływu na stan pacjentów w grupie kontrolnej, spożywającej wodę mineralną. Odsetek osób ze znaczną poprawą samopoczucia wynikającą ze zmniejszenia dolegliwości był istotnie statystycznie wyższy w grupie spożywającej wodę na bazie głębinowej wody morskiej w porównaniu z grupą kontrolną (p<0,05).
3.2.2.2. Analiza stężeń sIgA i produktów gnilnych w próbkach kału
Po zakończeniu przyjmowania interwencji, stężenie sIgA wzrosło w grupie badawczej, natomiast w grupie kontrolnej uległo obniżeniu w porównaniu z wartościami wyjściowymi. W celu oceny trwałego wpływu interwencji na status immunologiczny jelit przeprowadzono szczegółową analizę danych wyjściowych, dzieląc uczestników na dwie podgrupy w zależności od wartości mediany sIgA: niski (<500 µg/g) oraz wysoki (≥500 µg/g). Stężenie sIgA wykazało istotny statystycznie wzrost w obu podgrupach o niskich wartościach wyjściowych. Odwrotną tendencję zaobserwowano w podgrupach o wysokich wartościach wyjściowych: w grupie kontrolnej stężenie sIgA uległo istotnemu obniżeniu, natomiast w grupie badawczej pozostało na zbliżonym poziomie (Rycina 3).
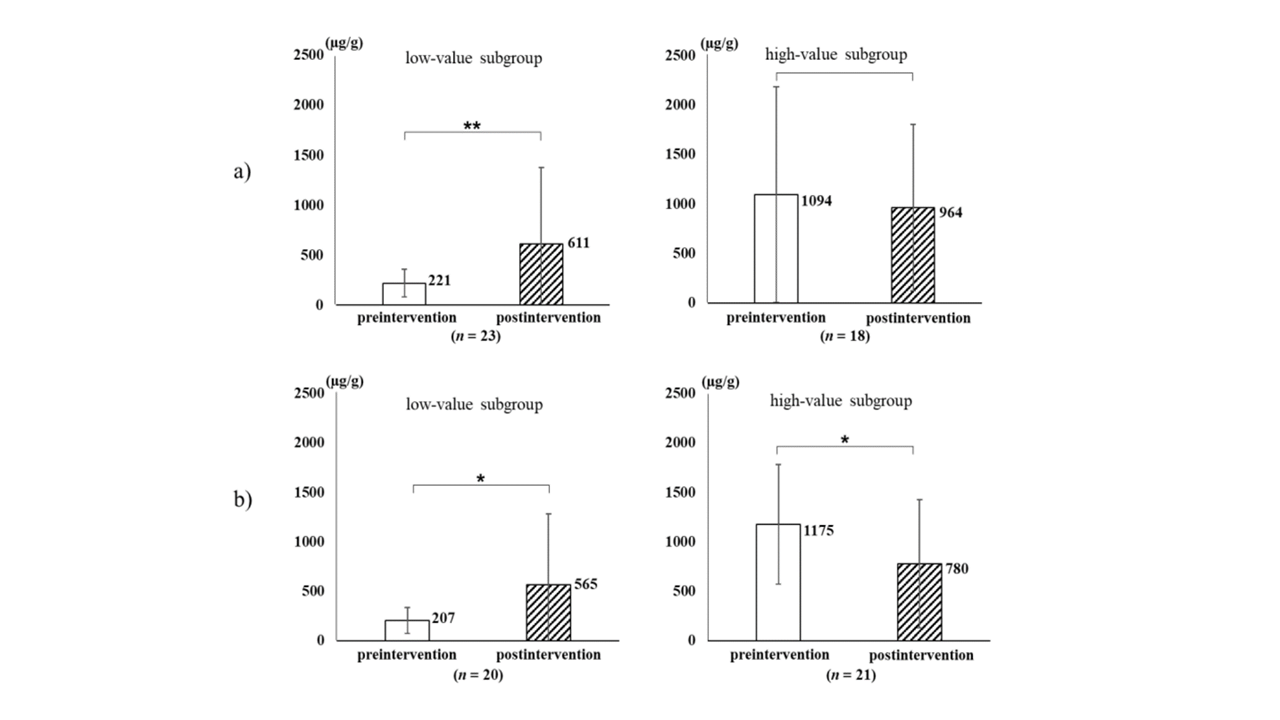
Rycina 3. Różnice w zmianach stężenia sIgA w trakcie trwania interwencji w grupie badawczej (a) i w grupie kontrolnej (b), w zależności od podgrupy (źródło: Takeuchi i wsp., 2022). Słupek biały – wartość przed zastosowaniem interwencji; słupek kreskowany – wartość po zastosowaniu interwencji. *p<0,05; **p<0,01.
Wśród produktów gnilnych w okresie po stosowaniu interwencji stwierdzono istotny wzrost stężenia indolu w grupie badawczej oraz fenolu w grupie kontrolnej. Średnie wartości stężeń sIgA i produktów gnilnych w kale w obu grupach terapeutycznych w trakcie stosowania interwencji zestawiono w poniższej tabeli.
Tabela 4. Średnie wartości stężenia sIgA i produktów gnilnych w kale w obu grupach terapeutycznych przed i po zastosowaniu interwencji (źródło: Takeuchi i wsp., 2022).
zastosowaniem interwencji
(209; 651)
(0,50; 6,67)
(9,15; 69,45)
(1,62; 4,15)
(11,80; 31,75)
(1,20; 7,80)
zastosowaniu interwencji
(319; 1039)
(0,85; 6,20)
(12,60; 95,72)
(0,70; 2,20)
(14,57; 41,10) ↑*
(1,30; 6,85)
zastosowaniem interwencji
(169; 1042)
(0,60; 7,20)
(21,20; 90,97)
(0,70; 2,90)
(11,85; 35,90)
(1,35; 10,00)
zastosowaniu interwencji
(215; 893)
(0,75; 4,70) ↑*
(18,22; 105,77)
(0,75; 8,45)
(8,50; 28,45)
(2,30; 14,75)
* p<0,05; ↑ – wzrost; IQR – zakres międzykwartylowy (ang. interquartile range).
3.2.2.3. Analiza stężeń krótkołańcuchowych kwasów tłuszczowych (SCFA) w próbkach kału
Analiza wykazała, że po zakończeniu stosowania interwencji, w przypadku kilku mniej licznych SCFA zaobserwowano niewielkie wahania ich stężeń (zarówno wzrosty, jak i spadki). W szczególności stężenia kwasu bursztynowego i mlekowego uległy obniżeniu w grupie badawczej, natomiast nie zmieniły się istotnie statystycznie w grupie kontrolnej. Ogółem jednak różnice w zmianach stężeń dziewięciu SCFA pomiędzy obiema grupami były zbliżone. Średnie wartości stężeń krótkołańcuchowych kwasów tłuszczowych (SCFA) w kale w obu grupach terapeutycznych w trakcie stosowania interwencji zestawiono w poniższej tabeli.
Tabela 5. Średnie wartości stężeń krótkołańcuchowych kwasów tłuszczowych (SCFA) w kale w obu grupach terapeutycznych w trakcie stosowania interwencji (źródło: Takeuchi i wsp., 2020).
zastosowaniem interwencji
(0,09; 0,46)
(0,08; 0,68)
(1,85; 4,02)
(0,75; 1,28)
(0,12; 0,20)
(0,14; 0,26)
(0,14; 0,26)
(0,13; 0,31)
zastosowaniu interwencji
(0,080; 0,220) ↓**
(0,10; 0,24) ↓*
(1,94; 4,21)
(0,81; 1,53)
(0,12; 0,20)
(0,51; 1,11)
(0,14; 0,33)
(0,14; 0,27)
zastosowaniem interwencji
(0,08; 0,23)
(0,08; 0,17)
(1,97; 3,66)
(0,87; 1,57)
(0,13; 0,19)
(0,54; 1,48)
(0,15; 0,27)
(0,14; 0,29)
zastosowaniu interwencji
(0,085; 0,345) ↑*
(0,08; 0,53)
(1,72; 3,20)
(0,67; 1,26) ↓**
(0,12; 0,21)
(0,33; 1,04) ↓**
(0,17; 0,34)
(0,15; 0,32)
* p<0,05; ** p<0,01; ↑ – wzrost; ↓ – spadek; SCFA – krótkołańcuchowe kwasy tłuszczowe (ang. short-chain fatty acids, SCFA); IQR – zakres międzykwartylowy (ang. interquartile range).
Z kolei łączna ilość trzech głównych SCFA — kwasu octowego, propionowego i masłowego — nieznacznie wzrosła w okresie po interwencji w grupie badawczej, podczas gdy w grupie kontrolnej odnotowano ich spadek (p<0,1), przy czym różnica pomiędzy grupami wyniosła 23% (Rycina 3a). Odsetek uczestników, u których po interwencji zaobserwowano wzrost stężeń trzech głównych SCFA, był istotnie wyższy w grupie badawczej niż w grupie kontrolnej, (Rycina 3b).
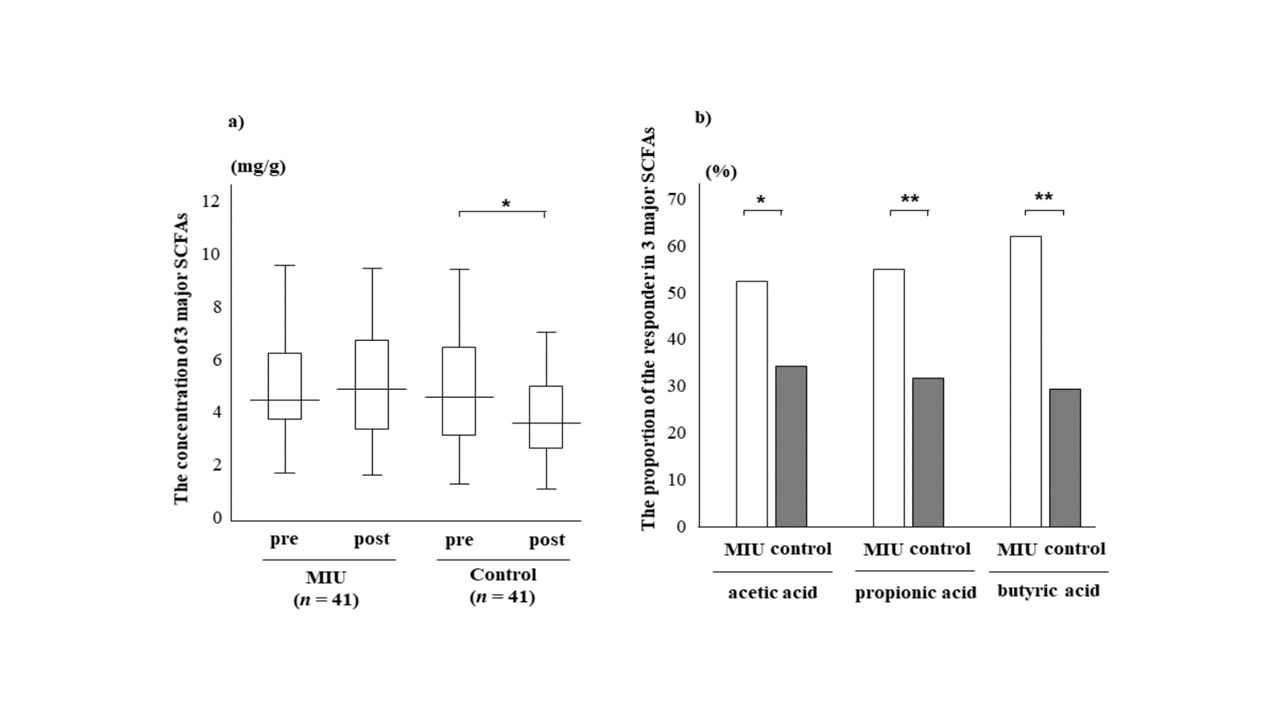
Rycina 4. Zmiana stężenia krótkołańcuchowych kwasów tłuszczowych (SCFA) w kale (a) oraz (b) odsetek uczestników, u których po zastosowaniu interwencji odnotowano wzrost stężenia SCFA (źródło: Takeuchi i wsp., 2022). (a) Górna i dolna krawędź każdego pudełka przedstawiają odpowiednio 75. i 25. percentyl, a linia wewnątrz pudełka oznacza medianę. Wąsy wykresu przedstawiają wartości minimalne i maksymalne. pre – przed interwencją; post – po interwencji. (b) *p < 0,05; **p < 0,01.
Na podstawie różnic w zmianach stężeń biomarkerów kałowych w przebiegu interwencji przeprowadzono analizę regresji logistycznej wielorakiej w celu oceny zależności pomiędzy rodzajem spożywanej wody a profilami biomarkerów kałowych. Wyniki wykazały, że spożywanie wody pitnej MIU (tj. na bazie głębinowej wody morskiej) miało istotny wpływ jedynie na jeden biomarker — kwas masłowy. Ponadto stwierdzono, że woda MIU wywierała wyraźniejszy wpływ na stężenia trzech głównych krótkołańcuchowych kwasów tłuszczowych (SCFA) w jelicie. Wśród 82 uczestników, kwas mrówkowy wykryto jedynie w niewielkiej liczbie próbek, w zakresie 0,01–0,02 mg/mL (granica detekcji: 0,01 mg/mL), co sugeruje, że w ludzkim jelicie powstają jedynie śladowe ilości tego związku.
3.2.2.4. Analiza stężeń izoflawonów w moczu
Wyniki stężenia izoflawonów w moczu, analizowano u 41 uczestników z grupy badawczej oraz 42 uczestników z grupy kontrolnej. Uczestników z wykrywalnym poziomem ekwolu ≥200 ng/mL klasyfikowano jako „producentów ekwolu”, natomiast osoby z niewykrywalnym stężeniem – jako „nie będących producentami ekwolu”, których wykluczono z analizy statystycznej.
W trakcie stosowania interwencji, ekwol wykryto w moczu 20 uczestników z grupy badawczej oraz 12 uczestników z grupy kontrolnej, którzy zostali zaklasyfikowani jako „producenci ekwolu”. Ogółem ekwol zidentyfikowano u 38,6% uczestników (32/83) a co istotne, spośród 32 „producentów”, 8 osób (6 z grupy badawczej i 2 z grupy kontrolnej) stało się „producentami” dopiero w trakcie trwania interwencji.
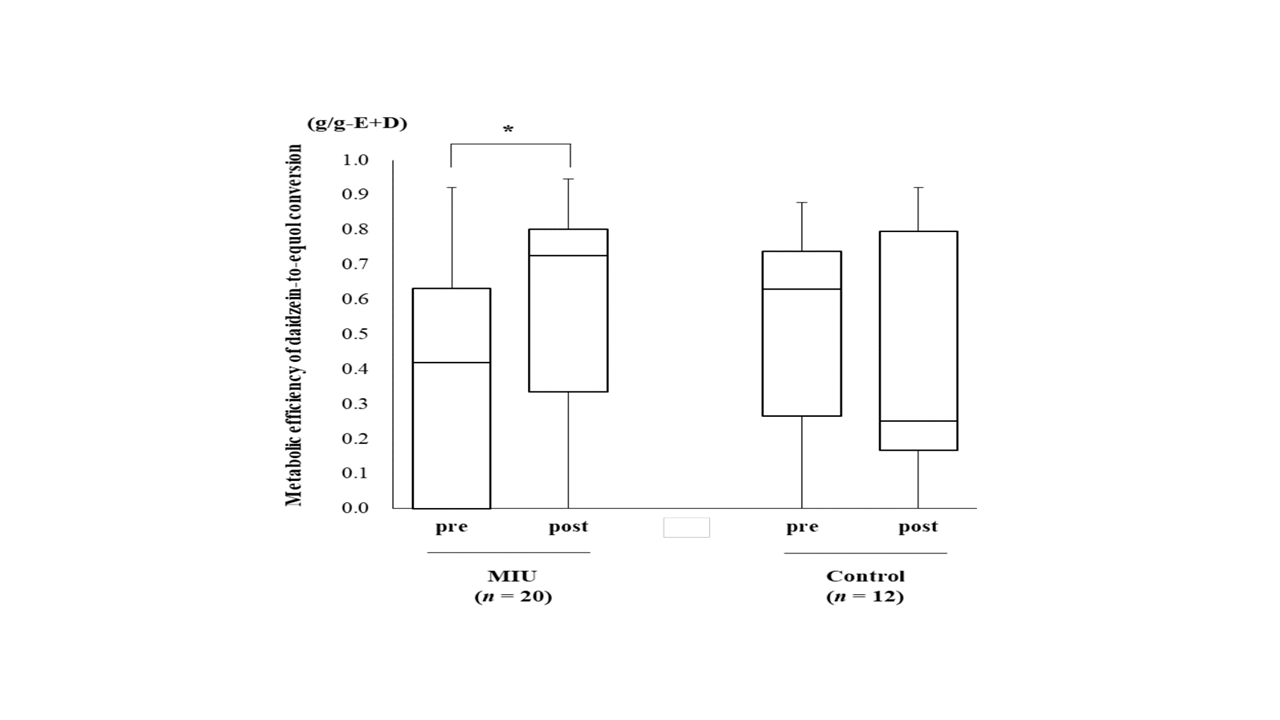
Rycina 5. Zmiana wydajności metabolicznej konwersji daidzeiny do ekwolu po zastosowaniu interwencji (źródło: Takeuchi i wsp., 2022). Górna i dolna krawędź każdego pola oznaczają 25. i 75. percentyl, a linia ciągła w polu oznacza medianę. Wąsy oznaczają wartości minimalne i maksymalne. przed, przed interwencją; po, po interwencji, * p<0,1.
Stężenie ekwolu korygowano względem zawartości kreatyniny (mg/g-Cre) oraz daidzeiny (g/g-D). Ponadto, obliczano wydajność metaboliczną konwersji daidzeiny do ekwolu, definiowaną jako stosunek ekwol / (ekwol + daidzeina) (g/g-E + D). Wydajność konwersji daidzeiny do ekwolu była istotnie statystycznie wyższa w grupie badawczej w porównaniu z grupą kontrolną (p<0,1) (Rycina 5). W poniższej tabeli przedstawiano wskaźniki wykrywalności izoflawonów w moczu. W przypadkach, gdy izoflawony nie były wykrywalne, ich stężenie przyjmowano jako zero.
Wyniki badania Takieuchi i wsp. (2022) wykazały, że spożywanie wody pitnej MIU (twardość na poziomie 88), na bazie głębinowej wody morskiej, powodowała niewielki wzrost łącznej ilości trzech głównych krótkołańcuchowych kwasów tłuszczowych (SCFA), jednak jej głównym działaniem było zwiększenie produkcji wydzielniczej immunoglobuliny A (sIgA) jako biomarkera kałowego. Dodatkowo MIU poprawiała wydajność metabolicznej konwersji daidzeiny do ekwolu, co przekładało się na korzystną modulację środowiska jelitowego.
4. Interpretacja dowodów klinicznych w kontekście zaprać, wzdęć i niestrawności
Wyniki badania Takeuchi i wsp. (2020) wykazały, że spożywanie rafinowanej głębinowej wody morskiej (RDSW) okazało się korzystniejsze niż picie konwencjonalnej wody mineralnej – zaparcia zostały złagodzone w znacznie większym stopniu w grupie pacjentów spożywających RDSW, czemu towarzyszyła zwiększona aktywność bakterii jelitowych uczestniczących w produkcji ekwolu oraz istotne zwiększenie stężenia krótkołańcuchowych kwasów tłuszczowych (SCFA) w kale i izoflawonów w moczu. Obecność SCFA pozytywnie wpływa na interakcje między gospodarzem a mikrobiotą jelitową, zapobiega różnorodnym zaburzeniom, działając poprzez receptory chemoatraktantów w narządach i komórkach, nawet w neuronach w mózgu [10].
Powszechnie przyjmuje się, że SCFA działają jako źródło energii i stymulują nabłonek jelita grubego a ich zwiększona produkcja wiąże się z lepszą perystaltyką jelit i krótszym czasem pasażu jelitowego, co może tłumaczyć obserwowaną poprawę zaparć. Wieloczynnikowa analiza regresji logistycznej wykazała, że spożywanie RDSW — lecz nie wody mineralnej — zwiększyło stężenie sześciu spośród dziewięciu analizowanych SCFA, a zwłaszcza stężenie kwasu octowego i propionowego. Kwas octowy wspomaga funkcję obronną komórek nabłonka gospodarza przed infekcją patogenną, tj. hamuje translokację toksyn [11], z kolei propionian stymuluje uwalnianie hormonów jelitowych o działaniu anorektycznym, peptydu YY oraz glukagonopodobnego peptydu-1 w komórkach okrężnicy. Hormony te zmniejszają apetyt i zapobiegają długotrwałemu przyrostowi masy ciała [12].
W badaniu Takeuchi i wsp. (2022) wykazano, że spożywanie wody MIU na bazie DSW doprowadziło do niewielkiego wzrostu łącznej ilości trzech głównych krótkołańcuchowych kwasów tłuszczowych, przy czym kluczowym obserwowanym efektem było istotne zwiększenie stężenia wydzielniczej immunoglobuliny A (sIgA) w kale, a podwyższony poziom był stale utrzymywany niezależnie od poziomu sIgA w okresie przed interwencją. Funkcjonalnie, sIgA jest dominującą immunoglobuliną wydzielaną do światła przewodu pokarmowego, odgrywa ważną rolę w ograniczaniu penetracji patogenów i kontroli kontaktu komensalnych bakterii z nabłonkiem jelitowym, co przyczynia się do modulowania odpowiedzi zapalnej i utrzymania równowagi mikrobioty [13]. Zwiększenie sIgA w świetle jelita jest uznawane za wskaźnik wzmocnienia lokalnej odporności błon śluzowych i stabilizacji interakcji między mikrobiotą a układem immunologicznym jelit – kluczowych elementów utrzymania homeostazy jelitowej oraz ochrony przed nadmierną reakcją zapalną.
Efekty zdrowotne izoflawonów, w tym ekwolu powstającego w jelicie w wyniku bakteryjnej konwersji daidzeiny, zależą od ilości i biodostępności wchłanianych składników odżywczych. Izoflawony są przekształcane do form aglikonowych (daidzeina i genisteina) z form glikozydowych (daidzin i genistin) przez enzymy, takie jak β-glukozydaza, obecne w mikroorganizmach jelitowych. Przyjmuje się, że izoflawony mogą łagodzić objawy różnych zespołów chorobowych, w tym nowotworów, chorób sercowo-naczyniowych, osteoporozy oraz objawów klimakterycznych. Dowody epidemiologiczne wykazują, że produkcja ekwolu jest związana z czynnikami środowiskowymi, nawykami żywieniowymi i składem mikrobioty, która w wyniku biotransformacji przekształca daidzeinę w ekwol.
W badaniu Takeuchi i wsp. (2020) wykazano, że stężenia ekwolu w moczu po spożywaniu RDSW uległy zwiększeniu, przy czym zmiana ta była co najmniej dwukrotnie większa niż w grupie kontrolnej. Wzrost stężenia dwóch innych izoflawonów (daidzeiny i genisteiny) zaobserwowano wyłącznie w grupie przyjmującej RDSW, a kierunek tych zmian był zgodny z obserwacjami dotyczącymi ekwolu, choć nie osiągnął istotności statystycznej.
Takeuchi i wsp. (2022), wykazali, że spożywanie MIU zwiększyło metaboliczną wydajność konwersji daidzeiny do ekwolu, co korzystnie wpłynęło na poprawę środowiska jelitowego. Spośród 15 bakterii produkujących ekwol wykrytych u 32 osób, względna liczebność B. ovatus wzrosła w grupie osób spożywających MIU, nie osiągając istotności statystycznej. Ponadto analiza mikrobioty kałowej pięciu uczestników, którzy stali się producentami ekwolu w całym okresie interwencji, wykazała, że proporcje B. wexlerae i S. cristatus znacznie wzrosły po zakończeniu stosowania interwencji. Wiadomo, że B. wexlerae zmniejsza stan zapalny związany z powikłaniami otyłości i produkuje kwas octowy jako końcowy produkt fermentacji glukozy [14]. Z kolei poprzednie badania nad S. cristatus wykazały, że peptydy S. cristatus hamują ekspresję genów wirulencji Porphyromonas gingivalis, co ma z kolei hamujący wpływ na stan mikrobioty jamy ustnej [15].
Wyniki obu badań wykazują, że spożycie wody na bazie DSW korzystnie moduluje funkcję jelit, co przejawia się zwiększoną produkcją krótkołańcuchowych kwasów tłuszczowych (SCFA), poprawą lokalnej odpowiedzi immunologicznej (sIgA) oraz redukcją niekorzystnych produktów przemiany bakteryjnej (np. fenolu). Choć w analizowanych badaniach nie zastosowano obiektywnych pomiarów wzdęć czy niestrawności, można wnioskować o potencjalnych korzyściach spożywania głębinowych wód morskich na podstawie znanych mechanizmów patofizjologicznych. Poprawa składu i aktywności mikrobioty jelitowej oraz zwiększenie produkcji SCFA sprzyjają ograniczeniu fermentacji proteolitycznej, która odpowiada za powstawanie gazów i toksycznych metabolitów drażniących śluzówkę. W efekcie może to prowadzić do złagodzenia subiektywnych objawów, takich jak wzdęcia, uczucie pełności czy dyskomfort po posiłku.
Co istotne z perspektywy patofizjologicznej, spożywanie wód o podwyższonej zawartości jonów magnezu i wapnia może indukować łagodny efekt prokinetyczny poprzez działanie osmotyczne i wpływ na napięcie mięśniówki gładkiej przewodu pokarmowego, co przypomina mechanizm działania soli magnezowych w środkach przeczyszczających, jednak przy mniejszym ryzyku efektów ubocznych. Warto także zaznaczyć, że efekty mogą być bardziej widoczne u osób z łagodnymi zaburzeniami niż u pacjentów z przewlekłą, oporną postacią zaparć.
5. Ograniczenia
Interpretując wyniki omawianych badań, należy uwzględnić istotne ograniczenia metodologiczne, które wpływają na siłę i zakres formułowanych wniosków. Po pierwsze, oba badania obejmowały stosunkowo krótki okres obserwacji (zaledwie 12 tygodni), co pozwala na ocenę wczesnych i krótkoterminowych zmian w biomarkerach jelitowych, lecz nie umożliwia wnioskowania o trwałości efektów ani ich długofalowych konsekwencjach zdrowotnych. Zarówno w przypadku stosowania RDSW, jak i MIU, próby badawcze obejmowały zdrowych dorosłych ochotników, co zwiększyło wewnętrzną spójność próby, ale ograniczyło możliwość uogólnienia wyników na populację kliniczną, tj. osoby z przewlekłymi zaburzeniami motoryki jelit, zespołem jelita wrażliwego, stanami zapalnymi, dysbiozą czy innymi zaburzeniami metabolicznymi. Ponadto, wielkość próby oraz analiza podgrup były ograniczone, co zmniejsza moc statystyczną i wiarygodność wniosków w obrębie podgrup.
Ograniczenia finansowe zaważyły na ograniczonym zakresie przeprowadzonych analiz laboratoryjnych, zawężając ocenę wyłącznie do biomarkerów obecnych w kale i moczu. W obu badaniach skoncentrowano się na wybranych parametrach środowiska jelitowego (m.in. krótkołańcuchowe kwasy tłuszczowe, sIgA oraz izoflawony), bez równoległej oceny szerokiego spektrum immunologicznych, metabolicznych i funkcjonalnych wskaźników ogólnoustrojowych oraz bez oceny markerów zapalnych, parametrów funkcji bariery jelitowej, poziomów SCFA we krwi ani fizjologicznych wskaźników perystaltyki. Zawartość SCFA w kale nie odzwierciedla ich realnej biodostępności ani stopnia absorpcji, co utrudnia zrozumienie mechanizmów działania na poziomie ogólnoustrojowym. Co więcej, nie przeprowadzono bezpośredniej analizy zależności między stężeniem poszczególnych minerałów a odpowiedzią metaboliczną, co utrudnia pełną interpretację danych.
Autorzy drugiego badania wyraźnie sugerują, że różnice w składzie mineralnym między zastosowaną interwencją eksperymentalną a standardową wodą kontrolną mogły być kluczowe dla wyników, ale nie zostały bezpośrednio zbadane.
6. Podsumowanie
Analiza zidentyfikowanych badań klinicznych jednoznacznie wskazuje, że spożywanie głębinowych wód morskich wywiera korzystny i wielokierunkowy wpływ na funkcjonowanie jelit. W przypadku stosowania obu interwencji, obserwowano istotny wzrost stężeń krótkołańcuchowych kwasów tłuszczowych (SCFA), które odgrywają kluczową rolę w regulacji motoryki jelit i łagodzeniu zaparć, utrzymaniu integralności bariery śluzówkowej i modulacji osi jelito-mózg. Wykazano, że spożywanie wody bogatej w minerały pochodzące z głębinowej wody morskiej (DSW) powodowało przyspieszenie konwersji daidzeiny do ekwolu oraz istotnie zwiększało sekrecję immunoglobuliny A (sIgA) w porównaniu z grupą kontrolną, co potwierdza, że DSW wzmacnia lokalną odporność jelit w sposób specyficzny dla swojego profilu mineralnego.
Podsumowując, spożywanie wody pochodzącej z głębin morskich stanowi obiecujący element wspomagający terapię zaparć o łagodnym lub umiarkowanym charakterze, poprzez mechanizmy związane z produkcją SCFA, poprawą funkcji mikrobioty jelitowej oraz wspieraniem odpowiedzi immunologicznej błony śluzowej. Choć mechanizmy te mogą pośrednio przyczyniać się do redukcji wzdęć i uczucia dyskomfortu, dowody w tym obszarze pozostają ograniczone i wymagają dalszych badań. Z praktycznego punktu widzenia, poprawa jakości i składu wody może być rozważana jako jeden z kluczowych elementów strategii terapeutycznej i wartościowe uzupełnienie postępowania niefarmakologicznego, jednak nie powinna zastępować kompleksowej diagnostyki i leczenia przyczynowego – konieczne jest uwzględnienie diety, aktywności fizycznej i higieny wypróżnień, a także wykluczenie wtórnych przyczyn zaparć. Właściwa edukacja pacjenta, monitorowanie efektów oraz ostrożność w interpretacji wyników pozostają kluczowe.
Bibliografia
[1] Mohd Nani SZ, Majid FA, Jaafar AB, et al. Potential Health Benefits of Deep Sea Water: A Review. Evid Based Complement Alternat Med. 2016;2016:6520475.
O autorce
Kinga Krawczyk-Kopras – badaczka i autorka związana z Instytutem Zoologii i Badań Biomedycznych Uniwersytetu Jagiellońskiego. Specjalizuje się w analizie badań klinicznych, metodologii naukowej oraz zdrowiu publicznym. W swojej pracy łączy wiedzę biomedyczną z zaawansowaną analityką danych medycznych.
Na co dzień pracuje jako analityk danych medycznych, zajmując się oceną skuteczności i bezpieczeństwa leków oraz wyrobów medycznych. Jej praca opiera się na kompleksowych, systematycznych przeglądach literatury naukowej z wykorzystaniem precyzyjnych strategii wyszukiwawczych, wielowymiarowych analiz danych, opracowywaniu wyników badań oraz wykonywaniu podstawowych analiz statystycznych. Posiada także doświadczenie w korekcie językowej i redakcyjnej tekstów medycznych oraz pracy z dokumentacją źródłową.
Jako autorka i współautorka posiada w dorobku publikacje z zakresu farmakologii, zdrowia publicznego oraz zdrowia reprodukcyjnego, opublikowane w wiodących międzynarodowych czasopismach naukowych, m.in. Frontiers in Pharmacology, Reproduction, Fertility and Development oraz Biomedicine & Pharmacotherapy – w tym prace, w których występuje jako pierwszy autor.
W tworzeniu treści popularyzatorskich i eksperckich koncentruje się na tematach związanych z mikrobiomem, fizjologią układu pokarmowego oraz działaniem bioaktywnych składników środowiska naturalnego, opierając każdy tekst na rzetelnych danych naukowych i aktualnych badaniach.
